Articol
Navigarea în comparațiile indirecte în evaluările tehnologiilor medicale: Informații din evaluările AMNOG germane
În lumea complicată a evaluării tehnologiilor medicale, comparațiile indirecte sunt adesea resurse indispensabile pentru evaluarea noilor produse farmaceutice atunci când nu sunt disponibile dovezi directe. Acest articol aprofundează peisajul riguros al evaluărilor AMNOG germane, dezvăluind informații și priorități cheie care modelează viitorul inovației în domeniul sănătății.
Un prim pas esențial în procesul de HTA este de a demonstra că metodologia utilizată pentru a genera date comparative față de ACT este adecvată. Dacă Comitetul mixt federal (G-BA) acceptă metodologia, toate datele sunt luate în considerare în evaluarea beneficiului adăugat. Cu toate acestea, dacă un CI nu este acceptat, aceste date sunt ignorate, iar evaluarea beneficiului adăugat se bazează doar pe dovezi directe.
Criteriile de acceptare pentru CI sunt stricte, succesul depinzând adesea de circumstanțe speciale. Limitările metodologice, cum ar fi eterogenitatea între studii și prejudecățile inerente în dovezile de pe partea de comparare, pot introduce incertitudine în evaluările comparative. Este esențial ca cercetătorii și evaluatorii să abordeze în mod transparent aceste limitări și să folosească metodologii robuste pentru a îmbunătăți validitatea și fiabilitatea rezultatelor IC. Îndrumarea metodelor cu privire la cerințele pentru IC este furnizată de Institutul pentru Calitate și Eficiență în Îngrijirea Sănătății (IQWiG). În plus, dezvoltatorii de medicamente pot programa o întâlnire suplimentară cu G-BA pentru a obține mai multe informații despre metodologia adecvată. Acest articol explorează rezultatele analizelor recente ale CI în evaluările AMNOG germane, evidențiind criteriile stricte de acceptare și implicațiile pentru diferite domenii terapeutice.
Criteriile de acceptare pentru CI sunt stricte, succesul depinzând adesea de circumstanțe speciale. Limitările metodologice, cum ar fi eterogenitatea între studii și prejudecățile inerente în dovezile de pe partea de comparare, pot introduce incertitudine în evaluările comparative. Este esențial ca cercetătorii și evaluatorii să abordeze în mod transparent aceste limitări și să folosească metodologii robuste pentru a îmbunătăți validitatea și fiabilitatea rezultatelor IC. Îndrumarea metodelor cu privire la cerințele pentru IC este furnizată de Institutul pentru Calitate și Eficiență în Îngrijirea Sănătății (IQWiG). În plus, dezvoltatorii de medicamente pot programa o întâlnire suplimentară cu G-BA pentru a obține mai multe informații despre metodologia adecvată. Acest articol explorează rezultatele analizelor recente ale CI în evaluările AMNOG germane, evidențiind criteriile stricte de acceptare și implicațiile pentru diferite domenii terapeutice.
Metode
O căutare sistematică a CI a fost efectuată folosind o bază de date internă AMNOG care conține fiecare evaluare a beneficiilor publicată pe site-ul G-BA până în aprilie 2024. Evaluarea CI de către G-BA și beneficiile medicale adăugate asociate au fost obținute din baza de date. Această analiză cuprinzătoare a inclus 222 de evaluări ale beneficiilor finalizate, cuprinzând 334 de subpopulații.
Rezultate
Dintre cele 334 de subpopulații pentru care a fost prezentat un CI, domeniile terapeutice predominante au fost bolile oncologice (51,2%), metabolice (15,0%) și infecțioase (11,4%) (Figura 1). În 22,5% din cazuri, CI a fost acceptat de G-BA (Figura 2). Deficiențele metodologice și similitudinea insuficientă a studiilor comparate au fost principalele motive pentru respingerea unui CI de către G-BA (Figura 3).
Figura 1. CI în evaluarea beneficiilor germane în funcție de domeniul terapeutic
Criteriile riguroase ale G-BA asigură că sunt acceptate numai circuite integrate robuste și fiabile. Acest accent pe rigoarea metodologică este crucial pentru menținerea integrității proceselor HTA. De regulă, G-BA necesită comparații ajustate, cum ar fi IC, potrivit lui Bucher. Cu toate acestea, au fost identificate atât comparații ajustate, cât și neajustate între CI acceptate, în timp ce alte metode, cum ar fi meta-analizele de rețea sau potrivirea scorului de propensiune, nu au fost considerate adecvate din punct de vedere metodologic. În consecință, analiza bazei de date a arătat că comparațiile neajustate pot fi considerate acceptabile și în anumite circumstanțe, cum ar fi în populațiile foarte vulnerabile sau atunci când se confruntă cu provocări semnificative în domeniul terapeutic.
Figura 2. Acceptarea CI de către G-BA
De exemplu, în cazul infecției cronice cu virusul hepatitei C, terapiile combinate care conțin interferon au fost definite ca ACT înainte de 2014. Interferonii sunt asociați cu efecte secundare semnificative, inclusiv depresie și gânduri suicidare. Având în vedere succesul tratamentului care poate fi obținut cu medicamentele mai noi sofosbuvir și elbasvir/grazoprevir, împreună cu potențialul pentru durate mai scurte ale terapiei și evitarea efectelor secundare severe legate de interferon, s-a considerat necesar, din motive etice, să se ia în considerare studii necontrolate, cu un singur braț, în care aceste medicamente mai noi au fost comparate cu controalele istorice. Astfel, o comparație ajustată nu a fost fezabilă și, în acest caz, o comparație neajustată a fost acceptată de G-BA.
De asemenea, se acordă considerații speciale populațiilor extrem de vulnerabile, cum ar fi pacienții pediatrici sau cei cu boli rare. În aceste cazuri, este posibil ca RCT-urile să nu fie fezabile din punct de vedere etic. În contextul deficitului de lipază acidă lizozomală, de exemplu – o boală rară care duce de obicei la o mortalitate crescută în primul an de viață, fără alternative de tratament disponibile la momentul evaluării – producătorul a furnizat CI controale istorice pentru a depăși lipsa de dovezi comparative directe. G-BA a acceptat această metodologie și a concluzionat că rezultatele CI au exclus posibilitatea ca câștigul demonstrat în supraviețuirea globală să poată fi explicat doar prin incertitudinea metodologică. Prin urmare, G-BA a acordat un indiciu al unui beneficiu suplimentar necuantificabil pentru sebelipasa alfa. Acesta este un exemplu de acceptare a unui CI neajustat în circumstanțe excepționale suplimentare.
Figura 3. Motive pentru respingerea CI de către G-BA
Figura 1. CI în evaluarea beneficiilor germane în funcție de domeniul terapeutic
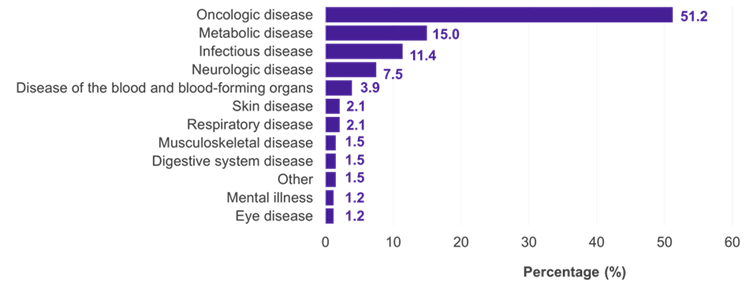
Cheie: IC – comparație indirectă.

Criteriile riguroase ale G-BA asigură că sunt acceptate numai circuite integrate robuste și fiabile. Acest accent pe rigoarea metodologică este crucial pentru menținerea integrității proceselor HTA. De regulă, G-BA necesită comparații ajustate, cum ar fi IC, potrivit lui Bucher. Cu toate acestea, au fost identificate atât comparații ajustate, cât și neajustate între CI acceptate, în timp ce alte metode, cum ar fi meta-analizele de rețea sau potrivirea scorului de propensiune, nu au fost considerate adecvate din punct de vedere metodologic. În consecință, analiza bazei de date a arătat că comparațiile neajustate pot fi considerate acceptabile și în anumite circumstanțe, cum ar fi în populațiile foarte vulnerabile sau atunci când se confruntă cu provocări semnificative în domeniul terapeutic.
Figura 2. Acceptarea CI de către G-BA
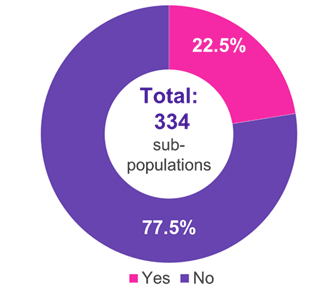
Cheie: G-BA – Comitetul Federal Mixt; IC – comparație indirectă.

De exemplu, în cazul infecției cronice cu virusul hepatitei C, terapiile combinate care conțin interferon au fost definite ca ACT înainte de 2014. Interferonii sunt asociați cu efecte secundare semnificative, inclusiv depresie și gânduri suicidare. Având în vedere succesul tratamentului care poate fi obținut cu medicamentele mai noi sofosbuvir și elbasvir/grazoprevir, împreună cu potențialul pentru durate mai scurte ale terapiei și evitarea efectelor secundare severe legate de interferon, s-a considerat necesar, din motive etice, să se ia în considerare studii necontrolate, cu un singur braț, în care aceste medicamente mai noi au fost comparate cu controalele istorice. Astfel, o comparație ajustată nu a fost fezabilă și, în acest caz, o comparație neajustată a fost acceptată de G-BA.
De asemenea, se acordă considerații speciale populațiilor extrem de vulnerabile, cum ar fi pacienții pediatrici sau cei cu boli rare. În aceste cazuri, este posibil ca RCT-urile să nu fie fezabile din punct de vedere etic. În contextul deficitului de lipază acidă lizozomală, de exemplu – o boală rară care duce de obicei la o mortalitate crescută în primul an de viață, fără alternative de tratament disponibile la momentul evaluării – producătorul a furnizat CI controale istorice pentru a depăși lipsa de dovezi comparative directe. G-BA a acceptat această metodologie și a concluzionat că rezultatele CI au exclus posibilitatea ca câștigul demonstrat în supraviețuirea globală să poată fi explicat doar prin incertitudinea metodologică. Prin urmare, G-BA a acordat un indiciu al unui beneficiu suplimentar necuantificabil pentru sebelipasa alfa. Acesta este un exemplu de acceptare a unui CI neajustat în circumstanțe excepționale suplimentare.
Figura 3. Motive pentru respingerea CI de către G-BA
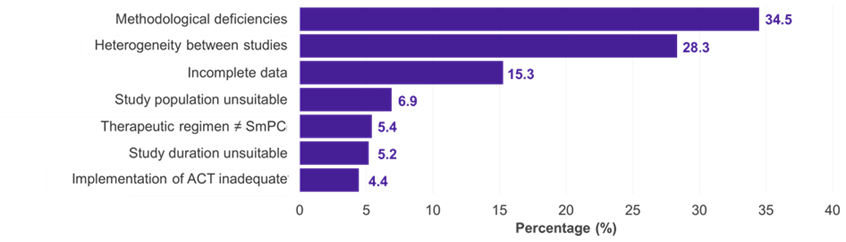
Cheie: ACT – terapie de comparare adecvată; G-BA – Comitetul Federal Mixt; IC – comparație indirectă; SmPC – rezumatul caracteristicilor produsului.


Concluzie
În concluzie, analiza CI în cadrul evaluărilor AMNOG germane evidențiază complexitatea și standardele ridicate necesare pentru astfel de evaluări. Criteriile stricte stabilite de G-BA asigură că sunt acceptate numai circuite integrate robuste și solide din punct de vedere metodologic, subliniind necesitatea unor abordări metodologice transparente și riguroase pentru a asigura validitatea și fiabilitatea rezultatelor. Deși doar un mic procent din CI sunt în cele din urmă acceptate, CI vor continua să furnizeze dovezi critice în contexte terapeutice specifice, cum ar fi populațiile vulnerabile.
Rezultatele ilustrează faptul că, în anumite circumstanțe, pot fi acceptate comparații ajustate și neajustate, în special atunci când considerentele etice exclud studiile directe directe și tratamentul pacienților cu boli rare sau severe este prioritar. Pe scurt și din punct de vedere al HTA, în primul rând este recomandabil să evaluați cu atenție fezabilitatea efectuării RCT-urilor. În cazurile în care un RCT nu este fezabil, CI sunt o metodă adecvată pentru a compensa lipsa de date comparative directe, dar alegerea unei metodologii adecvate este esențială. Pentru a maximiza probabilitatea de acceptare în contextul german, este recomandabil să respectați îndeaproape criteriile stricte ale G-BA.
Autori

Evaluările tehnologiilor medicale (HTA) sunt esențiale pentru determinarea valorii și impactului noilor produse farmaceutice asupra sistemelor de sănătate. În Germania, procesul AMNOG (Pharmaceuticals Market Reorganisation Act) impune companiilor farmaceutice să demonstreze beneficiul medical al medicamentelor nou aprobate împotriva unei terapii de comparație adecvate (ACT). Pentru a obține un beneficiu medical suplimentar, datele trebuie să demonstreze un avantaj al medicamentului evaluat față de ACT dincolo de un prag stabilit. În timp ce studiile controlate randomizate (RCT) sunt standardul de aur pentru dovezi, comparațiile indirecte (IC) devin adesea necesare atunci când comparațiile directe directe nu sunt fezabile.
Surse
-
Bucher HC, Guyatt GH, Griffith LE, et al. Rezultatele comparațiilor directe și indirecte ale tratamentului în meta-analiza studiilor controlate randomizate. J Clin Epidemiol. 1997; 50(6):683-691. https://dx.doi.org/10.1016/s0895-4356(97)00049-8
-
Comitetul federal mixt (G-BA). 2014. Frühe Nutzenbewertung: Beträchtlicher Zusatznutzen für Wirkstoff gegen chronische hepatitis C. Accesat la 31 octombrie 2024. https://www.g-ba.de/presse/pressemitteilungen-meldungen/546/
-
Comitetul federal mixt (G-BA). 2017. AM-RL-XII Elbasvir-Grazoprevir. Accesat la 31 octombrie 2024. https://www.g-ba.de/downloads/40-268-4429/2017-06-15_AM-RL-XII_Elbasvir-Grazoprevir_D-268_TrG.pdf
-
Comitetul federal mixt (G-BA). 2021. AM-RL-XII Sebelipase alfa. Accesat la 31 octombrie 2024. https://www.g-ba.de/downloads/40-268-7570/2021-06-03_AM-RL-XII_Sebelipase-alfa_D-606_TrG.pdf
-
Comitetul federal mixt (G-BA). 2024. Baza de date pentru evaluările beneficiilor. Accesat la 31 octombrie 2024. https://www.g-ba.de/
-
Institutul pentru Calitate și Eficiență în Îngrijirea Sănătății (IQWiG). 2023. Metode generale Versiunea 7.0. 19 septembrie 2023. https://www.iqwig.de/methoden/general-methods_version-7-0.pdf
-
Warmbold B, Scharrenbroich J, Teich K, Ingendoh-Tsakmakidis A, Löpmeier-Röh J, Kulp W. Comparații indirecte în evaluările AMNOG germane: păstrați credința. Prezentat la: Congresul European Anual ISPOR; Barcelona, Spania; 2024.
Acest articol rezumă înțelegerea Cencora asupra subiectului pe baza informațiilor disponibile public la momentul redactării acestui articol (a se vedea sursele enumerate) și a expertizei autorilor în acest domeniu. Este posibil ca recomandările furnizate în articol să nu fie aplicabile tuturor situațiilor și să nu constituie consultanță juridică; Cititorii nu ar trebui să se bazeze pe articol în luarea deciziilor legate de subiectele discutate.





