Artikkel
Navigere i indirekte sammenligninger i metodevurderinger: Innsikt fra tyske AMNOG-evalueringer
I den intrikate verdenen av medisinsk teknologivurdering er indirekte sammenligninger ofte uunnværlige ressurser for å evaluere nye legemidler når direkte bevis ikke er tilgjengelig. Denne artikkelen fordyper seg i det strenge landskapet av tyske AMNOG-evalueringer, og avslører nøkkelinnsikt og prioriteringer som former fremtiden for helseinnovasjon.
Et viktig første skritt i HTA-prosessen er å demonstrere at metoden som brukes til å generere komparative data kontra ACT, er hensiktsmessig. Hvis Federal Joint Committee (G-BA) aksepterer metodikken, blir alle data tatt i betraktning i mernyttevurderingen. Men hvis en IC ikke aksepteres, blir disse dataene sett bort fra, og vurderingen av merfordel er avhengig av direkte bevis alene.
Akseptkriteriene for IC-er er strenge, og suksess avhenger ofte av spesielle omstendigheter. Metodiske begrensninger, som heterogenitet på tvers av studier og iboende skjevheter i dokumentasjonen på komparatorsiden, kan introdusere usikkerhet i de komparative vurderingene. Det er viktig for forskere og evaluatorer å åpent adressere disse begrensningene og bruke robuste metoder for å forbedre gyldigheten og påliteligheten til IC-resultater. Metodeveiledning angående kravene til IC-er er gitt av Institute for Quality and Efficiency in Health Care (IQWiG). I tillegg kan legemiddelutviklere planlegge et ekstra rådgivningsmøte med G-BA for å få ytterligere innsikt i riktig metodikk. Denne artikkelen utforsker funnene fra nyere analyser av IC-er i tyske AMNOG-vurderinger, og fremhever de strenge kriteriene for aksept og implikasjonene for ulike terapeutiske felt.
Akseptkriteriene for IC-er er strenge, og suksess avhenger ofte av spesielle omstendigheter. Metodiske begrensninger, som heterogenitet på tvers av studier og iboende skjevheter i dokumentasjonen på komparatorsiden, kan introdusere usikkerhet i de komparative vurderingene. Det er viktig for forskere og evaluatorer å åpent adressere disse begrensningene og bruke robuste metoder for å forbedre gyldigheten og påliteligheten til IC-resultater. Metodeveiledning angående kravene til IC-er er gitt av Institute for Quality and Efficiency in Health Care (IQWiG). I tillegg kan legemiddelutviklere planlegge et ekstra rådgivningsmøte med G-BA for å få ytterligere innsikt i riktig metodikk. Denne artikkelen utforsker funnene fra nyere analyser av IC-er i tyske AMNOG-vurderinger, og fremhever de strenge kriteriene for aksept og implikasjonene for ulike terapeutiske felt.
Metoder
Et systematisk søk etter IC-er ble utført ved hjelp av en intern AMNOG-database som inneholder alle nyttevurderinger publisert på nettsiden til G-BA frem til april 2024. Vurderingen av IC-ene av G-BA og de tilhørende ekstra medisinske fordelene ble hentet fra databasen. Denne omfattende analysen inkluderte 222 fullførte nyttevurderinger som omfattet 334 underpopulasjoner.
Resultater
Blant de 334 underpopulasjonene som en IC ble presentert for, var de dominerende terapeutiske feltene onkologi (51,2 %), metabolske (15,0 %) og infeksiøse (11,4 %) sykdommer (figur 1). I 22,5 % av tilfellene ble IC akseptert av G-BA (figur 2). Metodiske mangler og utilstrekkelig likhet i de sammenlikte studiene var hovedårsakene til at G-BA avviste en IC (figur 3).
Figur 1. IC-er i tyske nyttevurderinger etter terapeutisk felt
G-BAs strenge kriterier sikrer at bare robuste og pålitelige IC-er aksepteres. Denne vektleggingen av metodisk stringens er avgjørende for å opprettholde integriteten til HTA-prosesser. Som regel krever G-BA justerte sammenligninger, for eksempel IC ifølge Bucher. Det ble imidlertid identifisert både justerte og ujusterte sammenligninger blant de aksepterte IC-ene, mens andre metoder, som nettverksmetaanalyser eller tilbøyelighetsskårematching, ikke ble vurdert som metodisk hensiktsmessige. Databaseanalysen viste derfor at ujusterte sammenligninger også kan anses som akseptable under visse omstendigheter, for eksempel i svært sårbare populasjoner eller når man står overfor betydelige utfordringer innen terapifeltet.
Figur 2. Aksept av IC-er av G-BA
For eksempel, når det gjelder kronisk hepatitt C-virusinfeksjon, ble interferonholdige kombinasjonsterapier definert som ACT før 2014. Interferoner er assosiert med betydelige bivirkninger, inkludert depresjon og selvmordstanker. Gitt behandlingssuksessen som kan oppnås med de nyere legemidlene sofosbuvir og elbasvir/grazoprevir, sammen med potensialet for kortere behandlingsvarighet og unngåelse av alvorlige interferonrelaterte bivirkninger, ble det av etiske grunner ansett som nødvendig å vurdere ukontrollerte, enarmsstudier der disse nyere legemidlene ble sammenlignet med historiske kontroller. Dermed var en justert sammenligning ikke mulig, og i dette tilfellet ble en ujustert sammenligning akseptert av G-BA.
Spesielle hensyn tas også til svært sårbare populasjoner, som pediatriske pasienter eller de med sjeldne sykdommer. I slike tilfeller kan det hende at RCTer ikke er etisk gjennomførbare å gjennomføre. I sammenheng med lysosomal sur lipasemangel, for eksempel – en sjelden sykdom som vanligvis resulterer i økt dødelighet i løpet av det første leveåret uten tilgjengelige behandlingsalternativer på vurderingstidspunktet – ga produsenten IC-er historiske kontroller for å overvinne mangelen på direkte komparativ bevis. G-BA aksepterte denne metodikken og konkluderte med at resultatene fra IC utelukket muligheten for at den demonstrerte gevinsten i total overlevelse bare kunne forklares med metodisk usikkerhet. G-BA ga derfor et hint om en ikke-kvantifiserbar tilleggsfordel for sebelipase alfa. Dette er et eksempel på aksept av en ujustert IC under ytterligere eksepsjonelle omstendigheter.
Figur 3. Årsaker til avvisning av IC-er av G-BA
Figur 1. IC-er i tyske nyttevurderinger etter terapeutisk felt
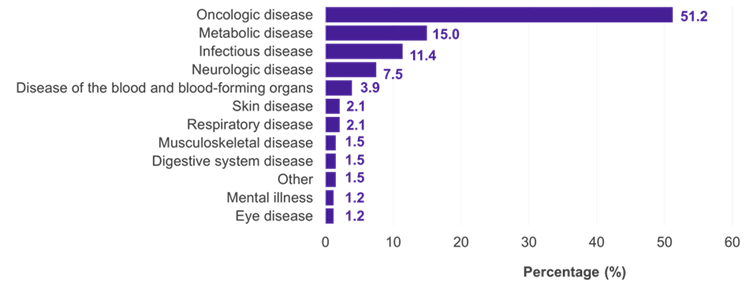
Nøkkel: IC – indirekte sammenligning.

G-BAs strenge kriterier sikrer at bare robuste og pålitelige IC-er aksepteres. Denne vektleggingen av metodisk stringens er avgjørende for å opprettholde integriteten til HTA-prosesser. Som regel krever G-BA justerte sammenligninger, for eksempel IC ifølge Bucher. Det ble imidlertid identifisert både justerte og ujusterte sammenligninger blant de aksepterte IC-ene, mens andre metoder, som nettverksmetaanalyser eller tilbøyelighetsskårematching, ikke ble vurdert som metodisk hensiktsmessige. Databaseanalysen viste derfor at ujusterte sammenligninger også kan anses som akseptable under visse omstendigheter, for eksempel i svært sårbare populasjoner eller når man står overfor betydelige utfordringer innen terapifeltet.
Figur 2. Aksept av IC-er av G-BA
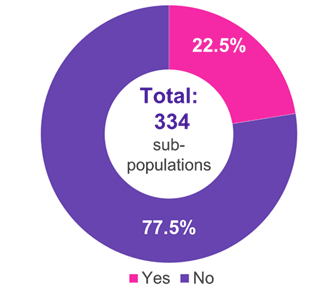
Nøkkel: G-BA – Føderal felleskomité; IC – indirekte sammenligning.

For eksempel, når det gjelder kronisk hepatitt C-virusinfeksjon, ble interferonholdige kombinasjonsterapier definert som ACT før 2014. Interferoner er assosiert med betydelige bivirkninger, inkludert depresjon og selvmordstanker. Gitt behandlingssuksessen som kan oppnås med de nyere legemidlene sofosbuvir og elbasvir/grazoprevir, sammen med potensialet for kortere behandlingsvarighet og unngåelse av alvorlige interferonrelaterte bivirkninger, ble det av etiske grunner ansett som nødvendig å vurdere ukontrollerte, enarmsstudier der disse nyere legemidlene ble sammenlignet med historiske kontroller. Dermed var en justert sammenligning ikke mulig, og i dette tilfellet ble en ujustert sammenligning akseptert av G-BA.
Spesielle hensyn tas også til svært sårbare populasjoner, som pediatriske pasienter eller de med sjeldne sykdommer. I slike tilfeller kan det hende at RCTer ikke er etisk gjennomførbare å gjennomføre. I sammenheng med lysosomal sur lipasemangel, for eksempel – en sjelden sykdom som vanligvis resulterer i økt dødelighet i løpet av det første leveåret uten tilgjengelige behandlingsalternativer på vurderingstidspunktet – ga produsenten IC-er historiske kontroller for å overvinne mangelen på direkte komparativ bevis. G-BA aksepterte denne metodikken og konkluderte med at resultatene fra IC utelukket muligheten for at den demonstrerte gevinsten i total overlevelse bare kunne forklares med metodisk usikkerhet. G-BA ga derfor et hint om en ikke-kvantifiserbar tilleggsfordel for sebelipase alfa. Dette er et eksempel på aksept av en ujustert IC under ytterligere eksepsjonelle omstendigheter.
Figur 3. Årsaker til avvisning av IC-er av G-BA
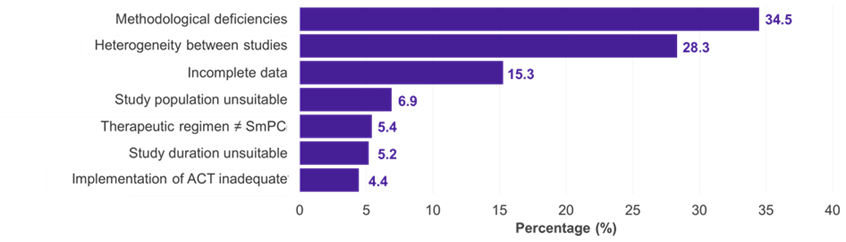
Nøkkel: ACT – passende komparatorterapi; G-BA – Føderal felleskomité; IC – indirekte sammenligning; Preparatomtale – preparatomtale – preparatomtale.


Konklusjon
Avslutningsvis fremhever analysen av IC-er innenfor rammen av tyske AMNOG-vurderinger kompleksiteten og de høye standardene som kreves for slike evalueringer. De strenge kriteriene satt av G-BA sikrer at bare robuste og metodisk forsvarlige IC-er aksepteres, og understreker nødvendigheten av transparente og strenge metodiske tilnærminger for å sikre validiteten og påliteligheten til resultatene. Selv om bare en liten prosentandel av IC-ene til slutt blir akseptert, vil IC-er fortsette å gi kritisk bevis i spesifikke terapeutiske sammenhenger som sårbare populasjoner.
Funnene illustrerer at justerte og ujusterte sammenligninger under visse omstendigheter kan aksepteres, spesielt når etiske hensyn utelukker direkte direkte head-to-head-studier, og behandling av pasienter med sjeldne eller alvorlige sykdommer prioriteres. Oppsummert og fra HTA-synspunktet er det tilrådelig å først nøye vurdere muligheten for å gjennomføre RCT-er. I tilfeller der en RCT ikke er gjennomførbar, er IC-er en egnet metode for å kompensere for mangelen på direkte komparative data, men valget av en passende metodikk er avgjørende. For å maksimere sannsynligheten for aksept i tysk sammenheng, er det tilrådelig å følge de strenge kriteriene til G-BA.
Forfattere

Metodevurderinger (HTA) er avgjørende for å fastslå verdien og virkningen av nye legemidler på helsevesenet. I Tyskland krever AMNOG-prosessen (Pharmaceuticals Market Reorganization Act) at farmasøytiske selskaper demonstrerer den medisinske fordelen av nylig godkjente legemidler mot en passende komparatorbehandling (ACT). For å oppnå en ekstra medisinsk fordel, må dataene demonstrere en fordel av det vurderte legemidlet fremfor ACT utover en fastsatt terskel. Mens randomiserte kontrollerte studier (RCT) er gullstandarden for bevis, blir indirekte sammenligninger (IC) ofte nødvendige når direkte direkte sammenligninger ikke er mulige.
Kilder
-
Bucher HC, Guyatt GH, Griffith LE, et al. Resultatene av direkte og indirekte behandlingssammenligninger i metaanalyse av randomiserte kontrollerte studier. J Clin Epidemiol. 1997; 50(6):683-691. https://dx.doi.org/10.1016/s0895-4356(97)00049-8
-
Føderal felleskomité (G-BA). 2014. Frühe Nutzenbewertung: Beträchtlicher Zusatznutzen für Wirkstoff gegen chronische hepatitt C. Åpnet 31 oktober 2024. https://www.g-ba.de/presse/pressemitteilungen-meldungen/546/
-
Føderal felleskomité (G-BA). 2017. AM-RL-XII Elbasvir-Grazoprevir. Åpnet 31 oktober 2024. https://www.g-ba.de/downloads/40-268-4429/2017-06-15_AM-RL-XII_Elbasvir-Grazoprevir_D-268_TrG.pdf
-
Føderal felleskomité (G-BA). 2021. AM-RL-XII Sebelipase alfa. Åpnet 31 oktober 2024. https://www.g-ba.de/downloads/40-268-7570/2021-06-03_AM-RL-XII_Sebelipase-alfa_D-606_TrG.pdf
-
Føderal felleskomité (G-BA). 2024. Database for fordelsvurderinger. Åpnet 31 oktober 2024. https://www.g-ba.de/
-
Institutt for kvalitet og effektivitet i helsevesenet (IQWiG). 2023. Generelle metoder versjon 7.0. 19. september 2023. https://www.iqwig.de/methoden/general-methods_version-7-0.pdf
-
Warmbold B, Scharrenbroich J, Teich K, Ingendoh-Tsakmakidis A, Löpmeier-Röh J, Kulp W. Indirekte sammenligninger i tyske AMNOG-vurderinger: behold troen. Presentert på: ISPOR årlige europeiske kongress; Barcelona, Spania; 2024.
Denne artikkelen oppsummerer Cencoras forståelse av emnet basert på offentlig tilgjengelig informasjon i skrivende stund (se oppførte kilder) og forfatternes ekspertise på dette området. Eventuelle anbefalinger gitt i artikkelen gjelder kanskje ikke for alle situasjoner og utgjør ikke juridisk rådgivning; Lesere bør ikke stole på artikkelen når de tar avgjørelser knyttet til temaene som diskuteres.





