Exploración de la logística y las modalidades de terapia génica y celular
Actualizado para el 3T 2024

Las terapias celulares y génicas (CGT) están dando forma al futuro de la medicina y ofrecen nuevas esperanzas a los pacientes de todo el mundo. Estas terapias avanzadas poseen el poder de atacar una amplia gama de afecciones. Sin embargo, es crucial reconocer que el panorama de la CGT es dinámico y que el éxito terapéutico requiere una cuidadosa consideración de múltiples factores a lo largo de todo el proceso de desarrollo y distribución de fármacos.
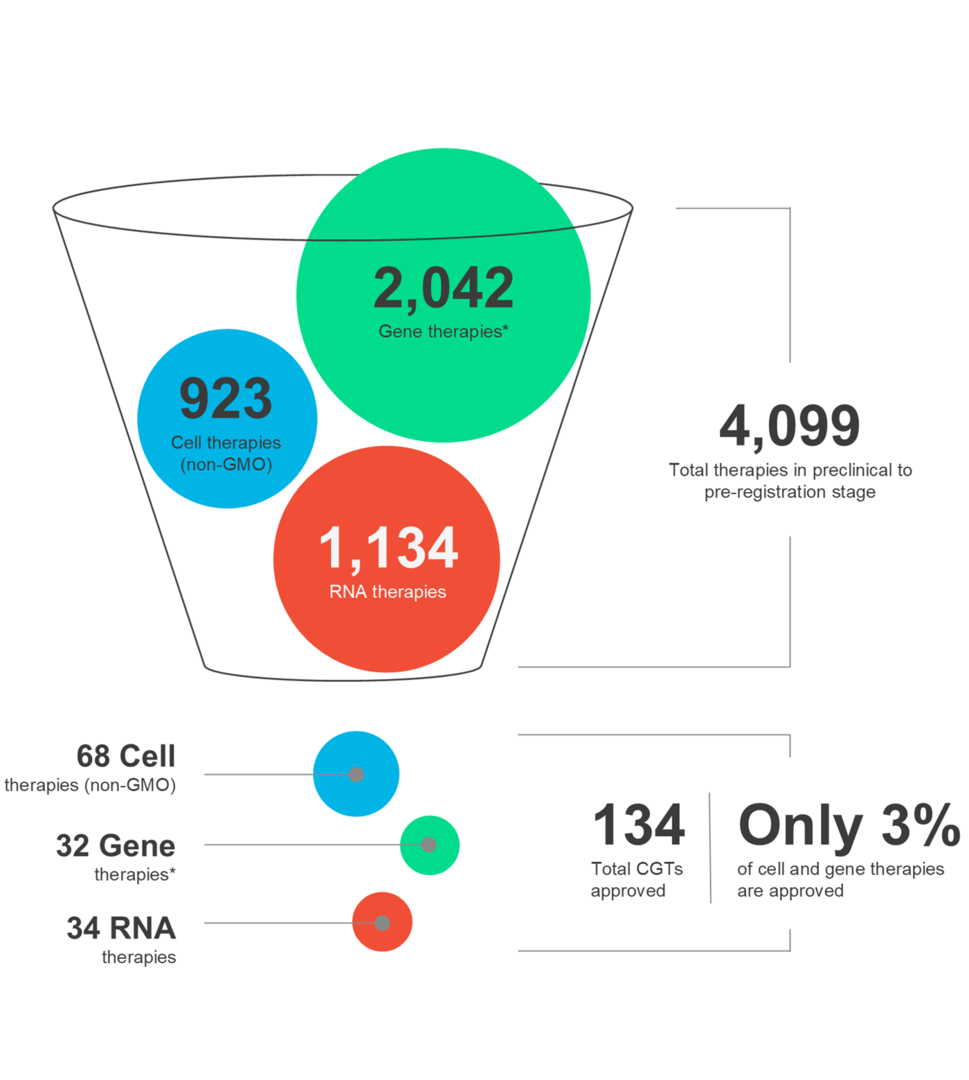
En nuestra infografía más reciente, explore las últimas tendencias del mercado y los matices de las diversas modalidades de CGT, junto con las terapias autólogas y alogénicas.

Preguntas frecuentes sobre la cartera de desarrollo de terapias celulares
¿Qué terapias celulares están aprobadas?
Hay muchas terapias celulares aprobadas, algunos ejemplos incluyen:
- Kymirah (tisagenlecleucel): Tipo de inmunoterapia conocida como terapia de células T con receptores de antígenos quiméricos (CAR-T), que se usa para tratar ciertos tipos de linfoma no Hodgkin y leucemia linfoblástica aguda
- Yescarta (axicabtagene ciloleucel): Terapia de células T con receptores de antígenos quiméricos que se usa para tratar linfomas grandes de células B después de dos o más líneas de terapia sistémica
- Provenza (sipuleucel-T): Inmunoterapia celular autóloga indicada para el tratamiento del cáncer de próstata metastásico resistente a la castración asintomático o mínimamente sintomático
¿Cuál es el proceso de aprobación de la terapia celular?
La aprobación de la terapia celular implica un proceso riguroso supervisado por organismos reguladores como la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés). Comienza con pruebas preclínicas en laboratorios y modelos animales, seguidas de una aplicación de nuevo fármaco en investigación (IND). Si se aprueba, los ensayos clínicos se llevan a cabo en tres fases para evaluar la seguridad, la eficacia y la dosis. Después del ensayo, se envía una Solicitud de Licencia de Productos Biológicos (BLA) para su revisión. Si tiene éxito, la terapia está aprobada para el mercado, pero continúa siendo monitoreada para detectar efectos a largo plazo.
¿Cuántas terapias celulares aprobadas existen?
El número de terapias celulares aprobadas puede variar según el país, ya que cada uno tiene sus propios organismos reguladores y procesos de aprobación. En Estados Unidos, las terapias celulares están reguladas por la FDA, mientras que en Europa están bajo el ámbito de la Agencia Europea de Medicamentos. Estas agencias tienen diferentes criterios y plazos de aprobación. Además, con los avances en la investigación médica y la tecnología, se desarrollan y prueban continuamente nuevas terapias celulares. En consecuencia, el número de terapias celulares aprobadas está creciendo constantemente en todo el mundo.




