4 spørsmål med Ben Penley

Diskutere behov for forhåndsgodkjenning av betalere og hvordan produsenter bedre kan møte dem


Hva har inspirert denne forskningen?
Loven om forhåndsgodkjenning av informasjonsutveksling (PIE) ble vedtatt i desember 2022. Det tok mye av det som ble spesifisert i Food and Drug Administrations (FDA) endelige veiledning om forhåndsgodkjenningskommunikasjon mellom betalere og produsenter og gjorde det til lov, og skapte en permanent trygg havn for produsenter til proaktivt å engasjere seg i PIE.
Vi ønsket å forstå, med vedtaket av PIE-loven, var det fortsatt et hull i forhåndsgodkjenningsinformasjonen betalerne mottok fra produsenter kontra hva de trengte for å ta beslutninger om formularer? Vi ønsket også å forstå at hvis dette gapet eksisterte, for hvilke typer informasjon var gapet mest utbredt?
Hva er de viktigste lærdommene fra forskningen din?
Undersøkelsen vår ble gjennomført i juni 2023. Av de 45 respondentene representerte 51 % helseplaner, 24 % representerte integrerte leveringsnettverk og 24 % representerte apotekfordelsforvaltere. Deres roller i disse organisasjonene ble delt mellom apotekdirektører (62 % og medisinske direktører (31 %, som de to ledende rollene. Når det gjelder geografi, var det en nesten jevn fordeling mellom nasjonale og regionale planer.
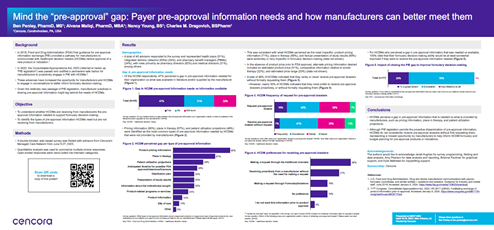
Vår første takeaway var at gapet fortsatt eksisterer – omtrent 50 prosent av betalerne indikerte at det var et hull i forhåndsgodkjenningsinformasjonen de trengte for å ta formelbeslutninger kontra det som var tilgjengelig for dem, enten gitt av produsenten eller offentlig tilgjengelig.
De ledende typene informasjon som dette gapet var til stede for var produktprisinformasjon (90 %), prognoser for pasientutnyttelse (48 %) og forventet tidslinje for FDA-godkjenning (38 %). Så å forstå kostnadene, forventet bruk og når behandlingen ville være tilgjengelig var de ledende typene forhåndsgodkjenningsinformasjon betalerne trengte, men ikke hadde mottatt.
Et annet viktig funn var knyttet til virkningen av å lukke gapet. Hvis betalerne hadde forhåndsgodkjenningsinformasjonen de trengte, ville beslutningstakingen deres bli forbedret? Kort sagt fant vi at ja, alle respondentene sa at beslutningstakingen deres ville bli forbedret.
Var det noe i forskningen som var overraskende, som du ikke forventet, som du fant ut?
Vi ble overrasket over at 50 % av betalerne fortsatt oppfattet et gap, selv om PIE-loven har vært lov i nesten 18 måneder. Videre sa bare 7 % av betalerne at de ofte mottok forhåndsgodkjenningsdossierer proaktivt. Vi mener at produsenter bør føle seg bemyndiget til å dele informasjon proaktivt med betalere slik at de kan ta mer informerte beslutninger.
Hva er de neste trinnene fra denne forskningen?
Vår neste undersøkelse relatert til dette emnet kommer til å se mer på resultatene av PIE. Vi vet at betalere vil ha denne informasjonen – vi vet at betalere trenger denne informasjonen. Vi ønsker nå å se på hva disse resultatene er for produsenter som lykkes med å engasjere seg i PIE.
Vi fant ut at alle betalere mente å lukke PIE-gapet ville forbedre deres formelbeslutningstaking. Men vi ønsker å forstå nøyaktig hvordan det vil bli forbedret. Vil det bare gjøre betalerne mer informerte? Vil betalerne kunne ta beslutninger raskere? Hvilken innvirkning vil det ha på hvordan et produkt vurderes? Det er noe vi planlegger å se nærmere på i fremtidig forskning.
Sitater som er relevante for innholdet beskrevet her, er gitt i artikkelen som er lenket til her. Lesere bør gjennomgå all tilgjengelig informasjon relatert til emnene nevnt her og stole på sin egen erfaring og ekspertise for å ta beslutninger relatert til dette.




