Hücre ve gen tedavisi lojistiğini ve modalitelerini keşfetmek
2024 Q3 için güncellendi

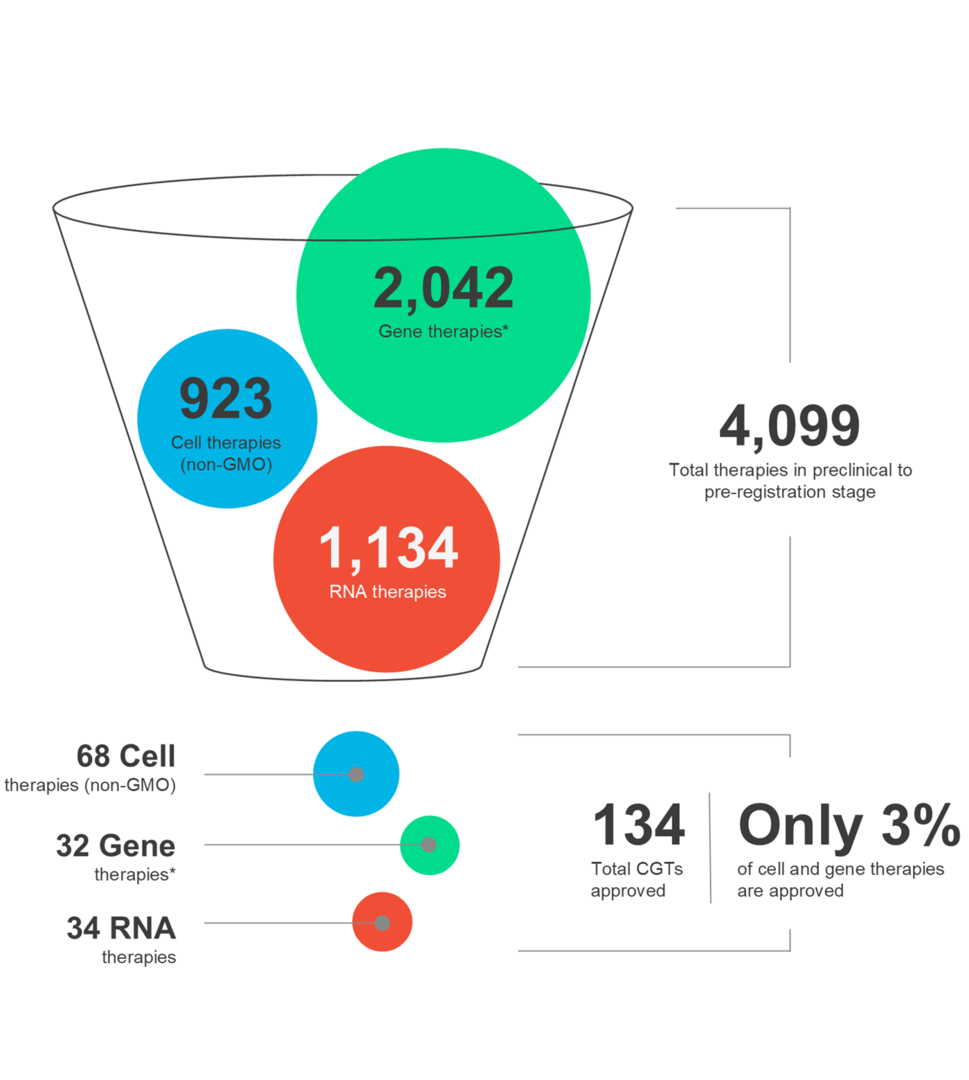
Hücre ve gen tedavileri (CGT'ler) tıbbın geleceğini şekillendiriyor ve dünya çapındaki hastalara yeni umutlar sunuyor. Bu gelişmiş tedaviler, çok çeşitli koşulları hedefleme gücüne sahiptir. Bununla birlikte, CGT ortamının dinamik olduğunu ve terapötik başarının tüm ilaç geliştirme ve dağıtım süreci boyunca birden fazla faktörün dikkatli bir şekilde değerlendirilmesini gerektirdiğini kabul etmek çok önemlidir.
En son infografiğimizde, otolog ve allojenik tedavilerin yanı sıra en son pazar trendlerini ve çeşitli CGT modalitelerinin nüanslarını keşfedin.

Hücre tedavisi geliştirme boru hattı SSS
Hangi hücre tedavileri onaylanmıştır?
Onaylanmış birçok hücre tedavisi vardır, bazı örnekler şunları içerir:
- Kymirah (tisagenlecleucel): CAR-T hücre tedavisi olarak bilinen bir tür immünoterapi ve belirli Hodgkin dışı lenfoma ve akut lenfoblastik lösemiyi tedavi etmek için kullanılır
- Yescarta (axicabtagene ciloleucel): İki veya daha fazla sistemik tedavi hattından sonra büyük B hücreli lenfomaları tedavi etmek için kullanılan bir CAR-T hücre tedavisi
- İntikam (sipuleucel-T): Asemptomatik veya minimal semptomatik metastatik kastrat dirençli prostat kanserinin tedavisi için endike otolog bir hücresel immünoterapi
Hücre tedavisi onay süreci nasıldır?
Hücre tedavisi onayı, Gıda ve İlaç Dairesi (FDA) gibi düzenleyici kurumlar tarafından denetlenen titiz bir süreci içerir. Laboratuvarlarda ve hayvan modellerinde klinik öncesi testlerle başlar, ardından araştırma amaçlı yeni bir ilaç (IND) uygulaması gelir. Onaylanırsa, güvenlik, etkinlik ve dozu değerlendirmek için klinik deneyler üç aşamada yürütülür. Duruşma sonrası, incelenmek üzere bir Biyolojik Lisans Başvurusu (BLA) sunulur. Başarılı olursa, tedavi pazar için onaylanır, ancak uzun vadeli etkiler için izlenmeye devam eder.
Kaç tane onaylanmış hücre tedavisi var?
Onaylanan hücre tedavilerinin sayısı, her birinin kendi düzenleyici kurumları ve onay süreçleri olduğu için ülkeye göre değişebilir. ABD'de hücre tedavileri FDA tarafından düzenlenirken, Avrupa'da Avrupa İlaç Ajansı'nın yetki alanına girerler. Bu ajansların onay için farklı kriterleri ve zaman çizelgeleri vardır. Ayrıca, tıbbi araştırma ve teknolojideki gelişmelerle birlikte, sürekli olarak yeni hücre tedavileri geliştirilmekte ve test edilmektedir. Sonuç olarak, onaylanmış hücre tedavilerinin sayısı dünya çapında giderek artmaktadır.




